Elektrochemická stabilita disubstituované imidazolové iontové kapaliny Ve vysokopěťovém nebo redox-aktivním prostředí je ovlivněna několika vzájemně propojenými mechanismy zakořeněnými v jejich molekulární struktuře a elektronické konfiguraci:
Elektronová delokalizace na imidazolovém kruhu: Aromatická povaha imidazolového kruhu umožňuje významnou delokalizaci π-elektronů, což zvyšuje rezistenci molekuly vůči oxidační nebo redukční degradaci. Při nahrazení na obou položkách 1- a 3 může být elektronická hustota redistribuována způsobem, který stabilizuje kation proti reakcím přenosu elektronů.
Účinky substituentu: Typ a poloha substituentů na imidazolovém kroužku významně ovlivňují elektrochemickou stabilitu. Skupiny s elektronem mohou zvýšit nukleofilitu a snížit oxidační stabilitu, zatímco skupiny pro smazání elektronů (jako jsou halogeny nebo nitrily) mohou zlepšit oxidační rezistenci stabilizací nejvyššího obsazeného molekulárního orbitálu (HOMO). Naopak, tyto skupiny mohou také snížit redukční potenciál stabilizací nejnižšího neobsazeného molekulárního orbitálu (LUMO), v závislosti na prostředí.
Sterická překážka a prostorové stínění: Objemné substituenty v poloze 1 a 3 mohou fyzicky chránit imidazoliový kroužek před nukleofilním nebo elektrofilním útokem, což omezuje nežádoucí boční reakce, které by se mohly vyskytnout za podmínek vysokého napětí.
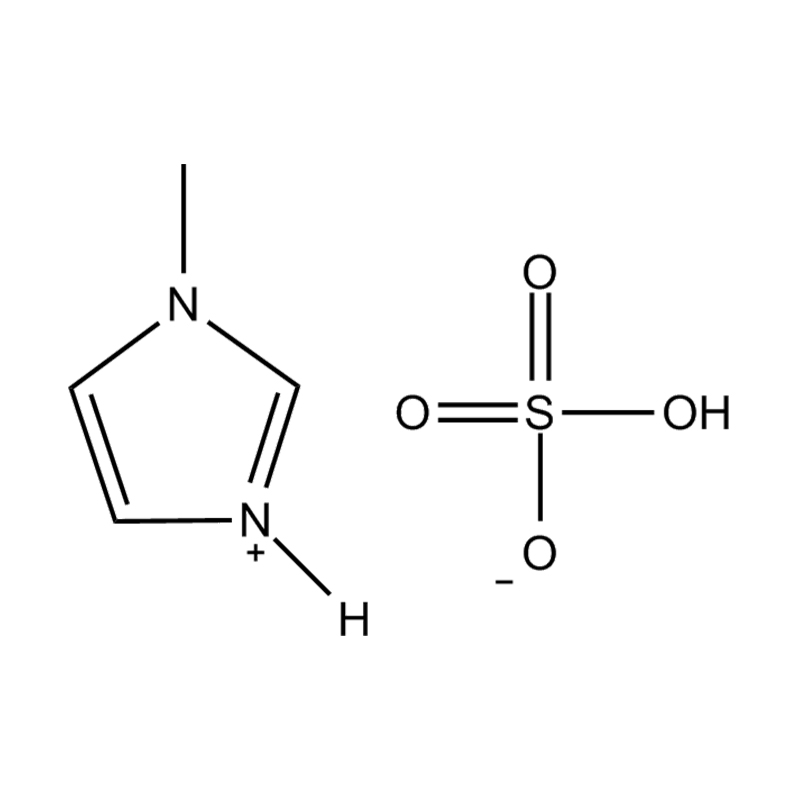
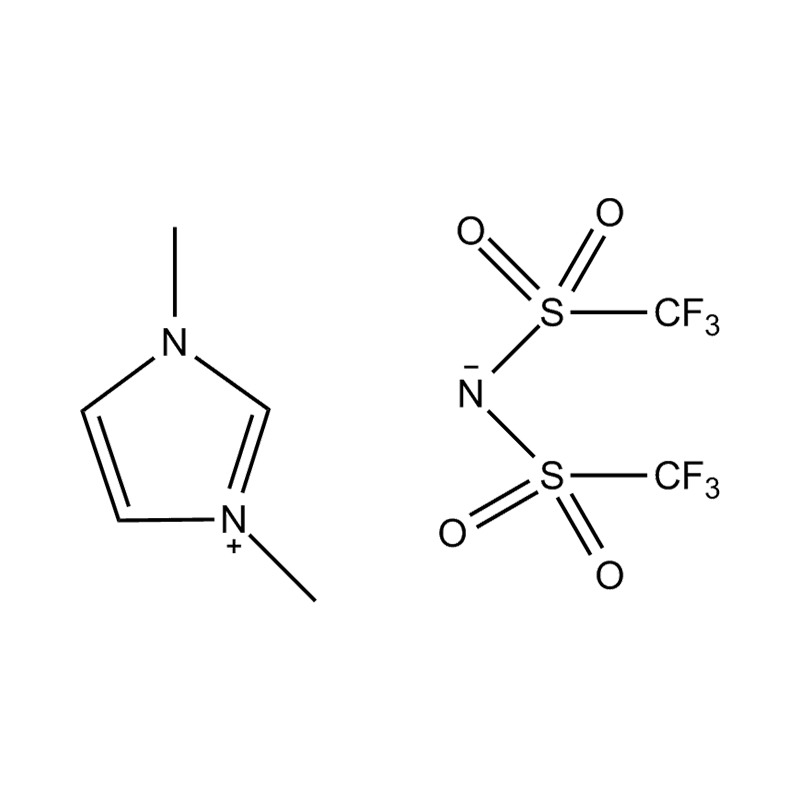
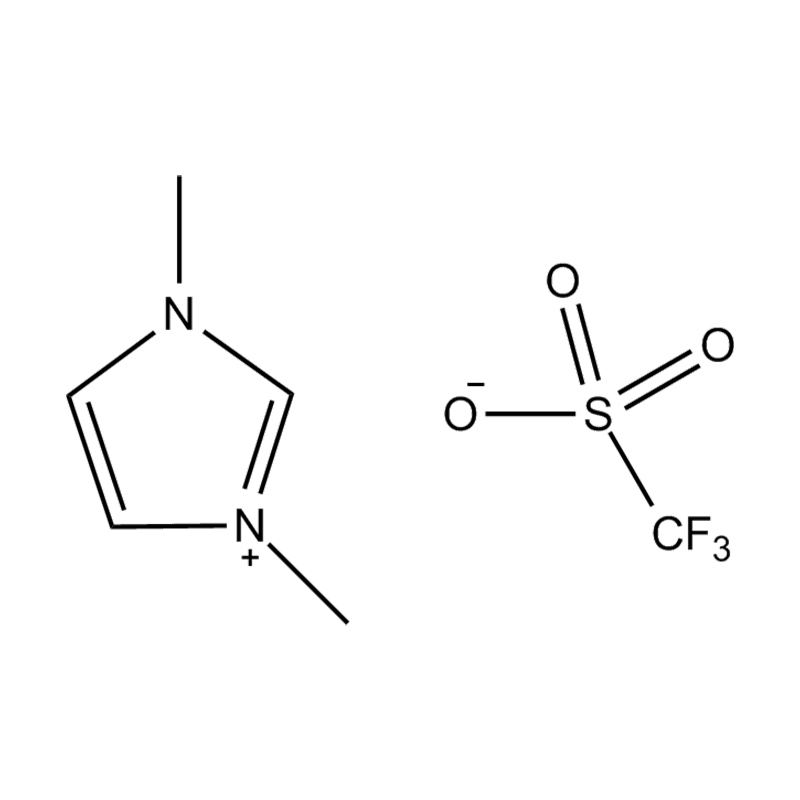
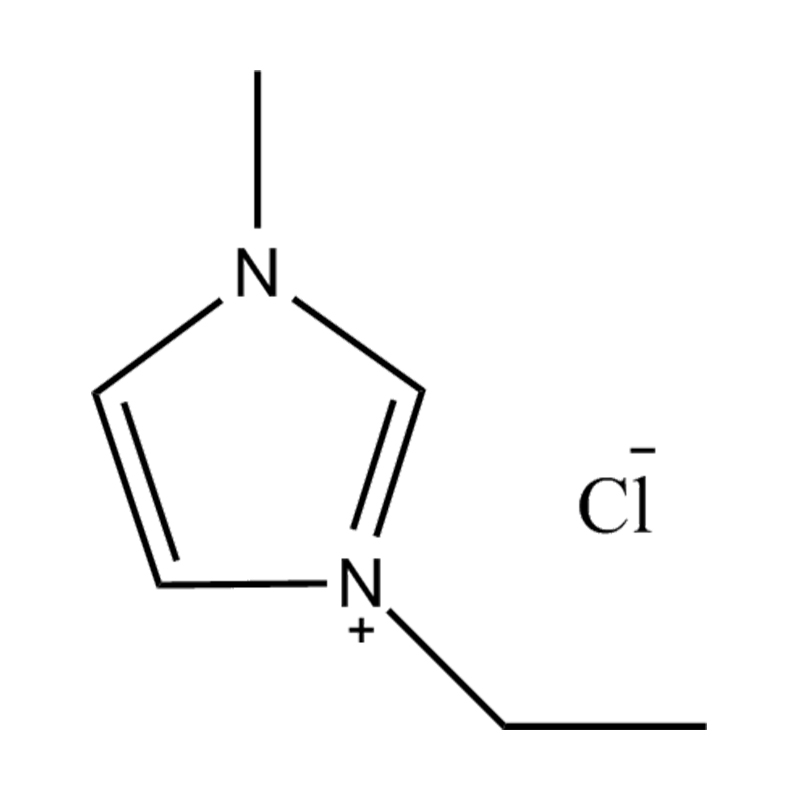
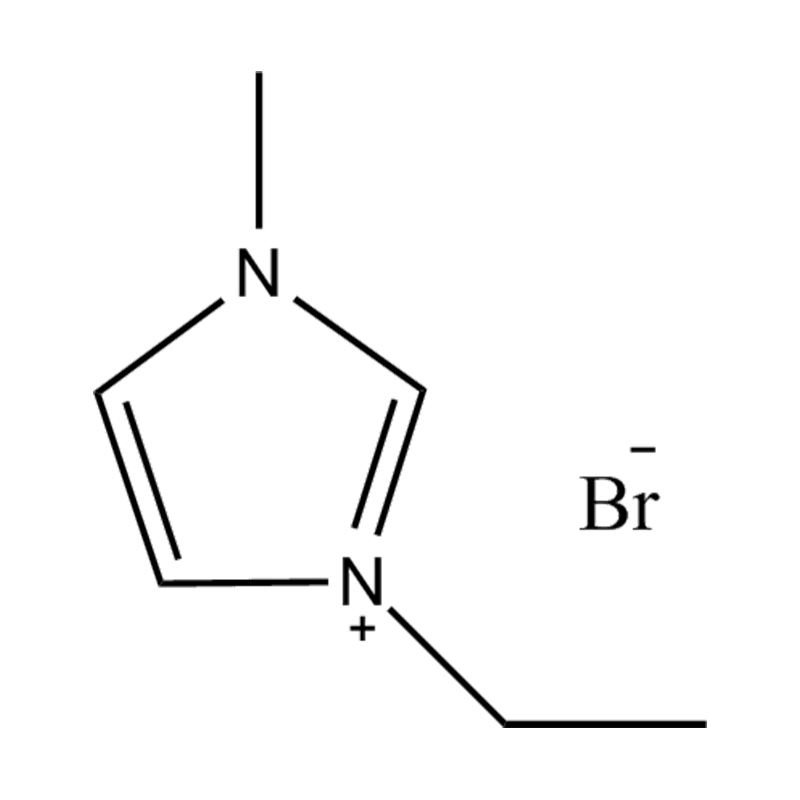
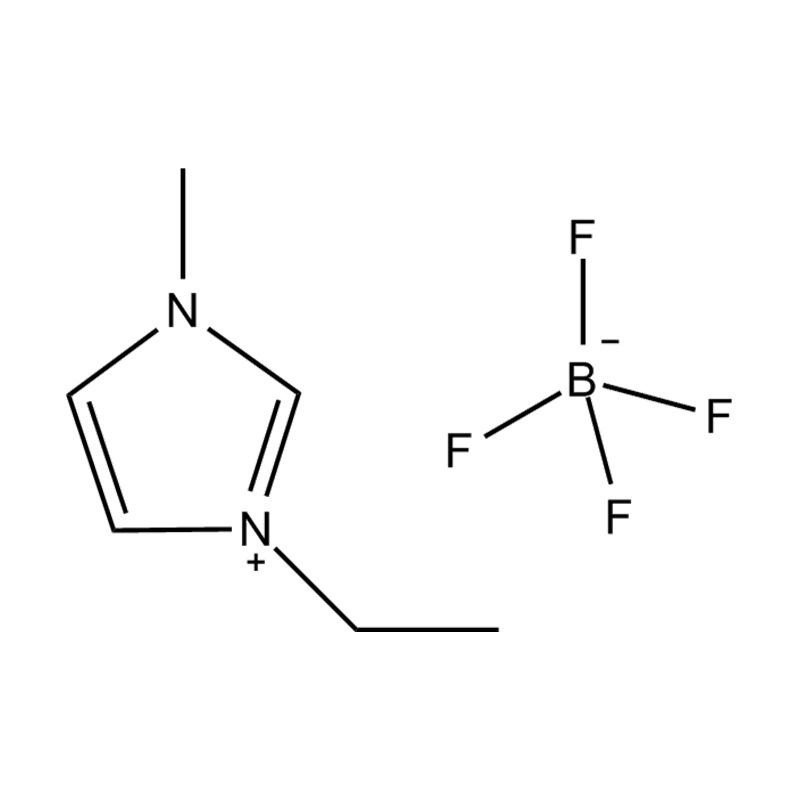
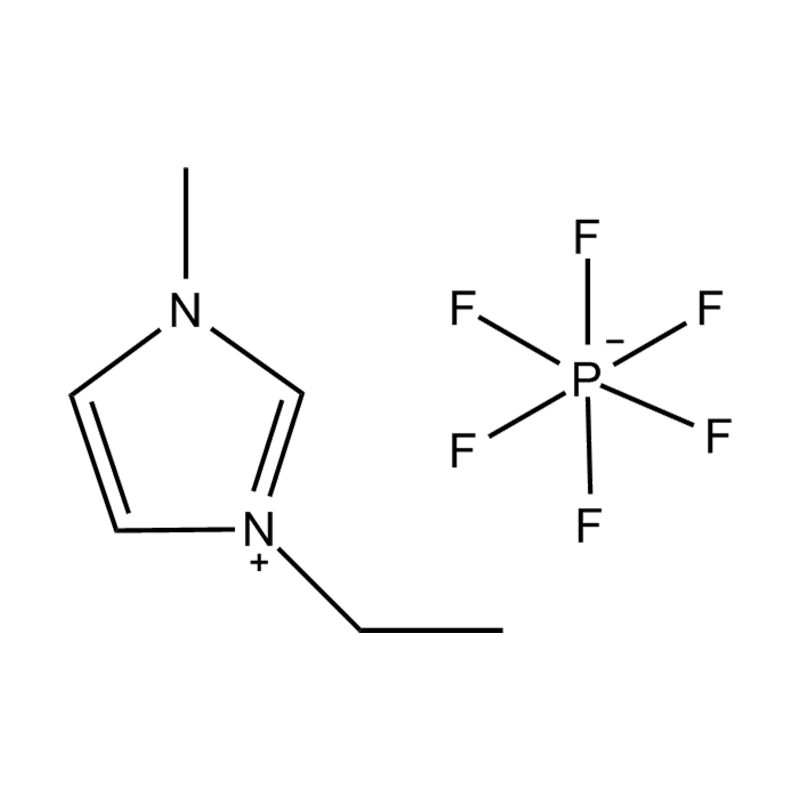
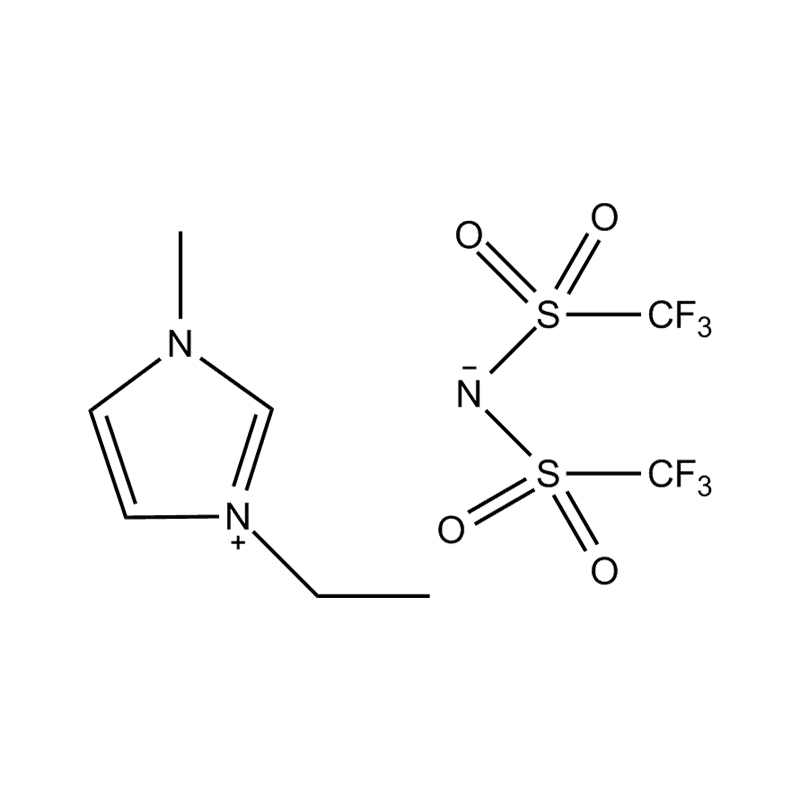
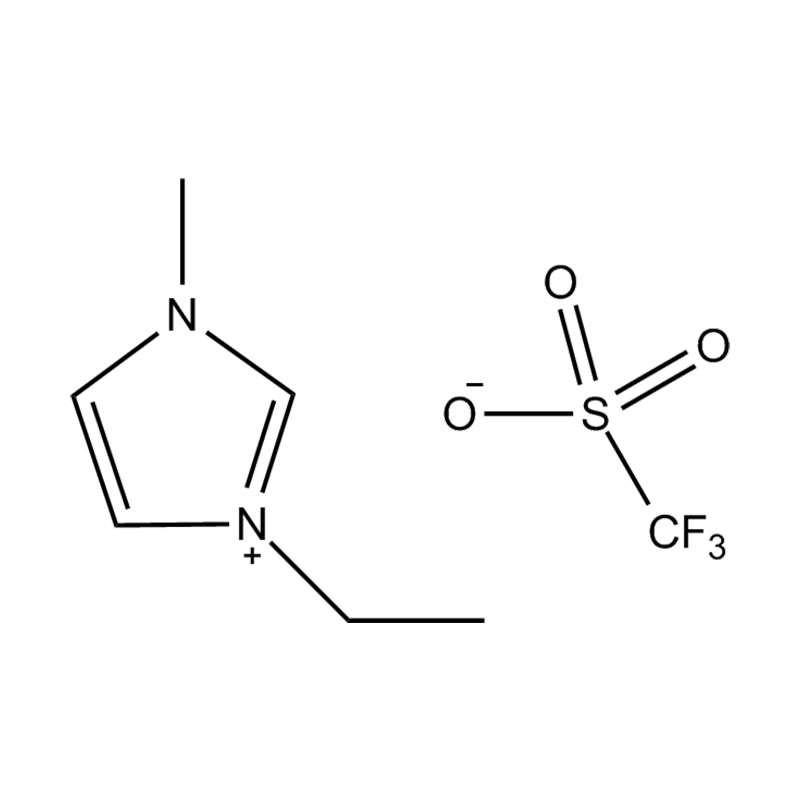
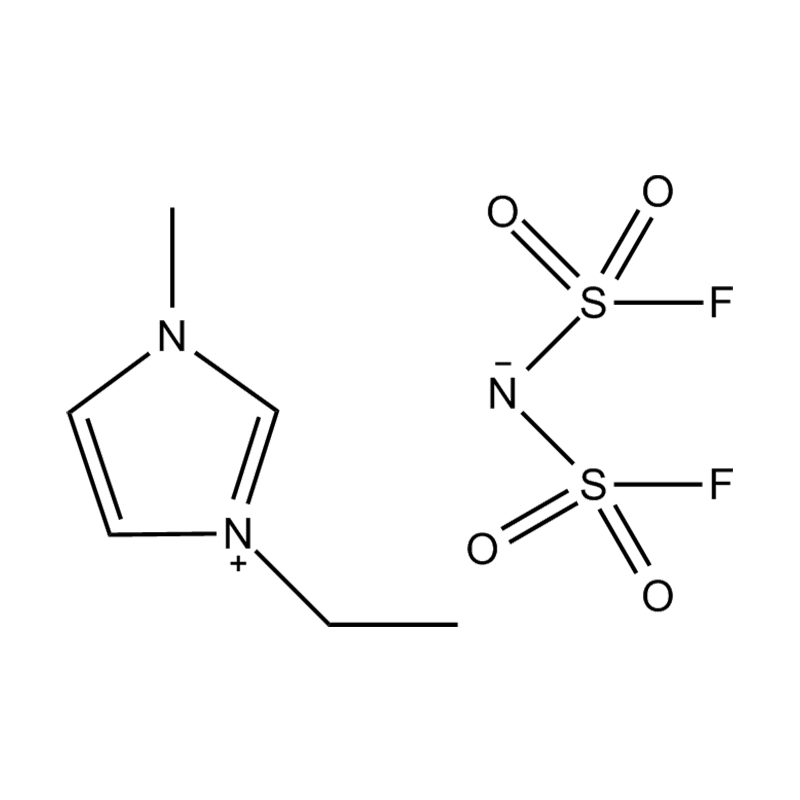
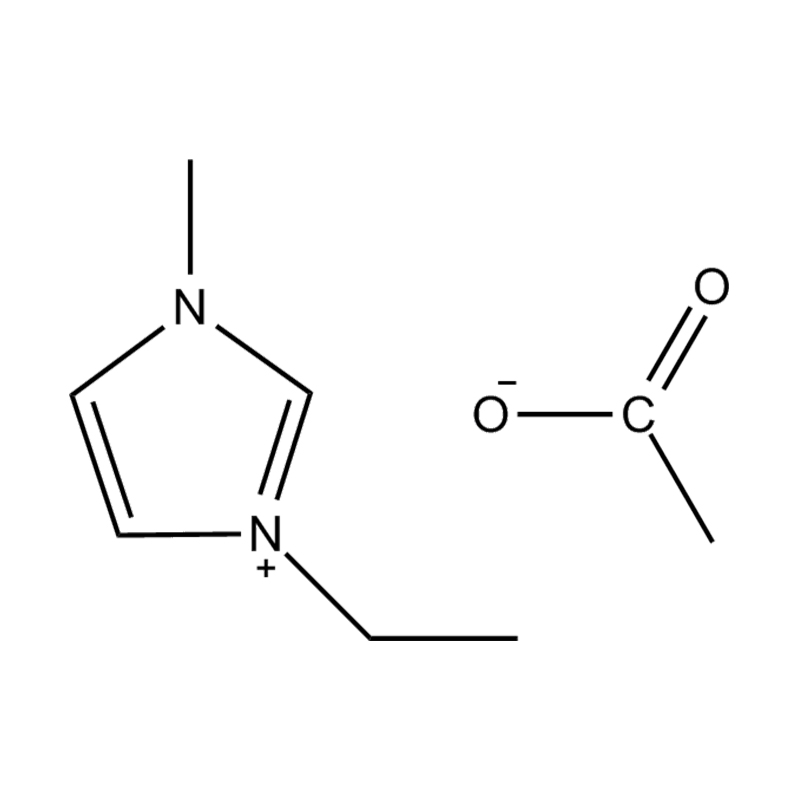
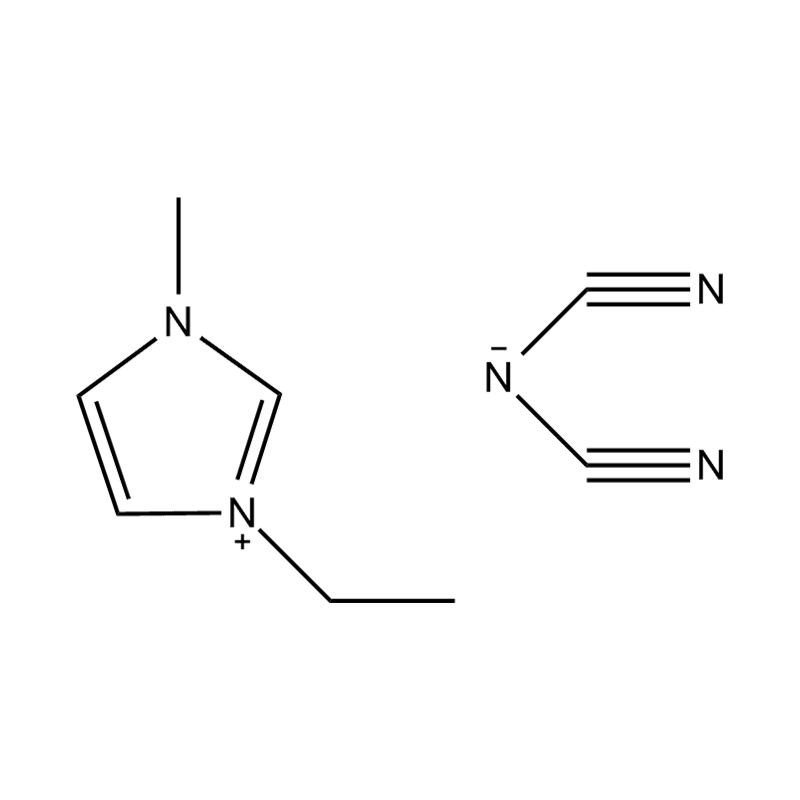
Stabilita páru aniontového kationtu: párování disubstituovaného kationtu imidazolium se stabilním, nekoordičním aniontem (např. BIS (trifluoromethylsulfonyl) Imide [tfsi⁻] nebo tetrafluoroboritate [bf₄⁻]) snižuje imiderovii a přispívání na šířkovou elektrickou okno. Tyto anionty odolávají rozkladu a udržují iontovou vodivost bez narušení redoxních reakcí.
Mobilita iontů a mezifázové chování: ve vysokopěťových systémech, zejména v elektrochemických zařízeních, ovlivňují mobilitu iontů a jejich organizace na elektrodových rozhraních. DisUbstituované ionické kapaliny imidazolu mohou tvořit dobře organizované mezifázové vrstvy, které zabraňují přímému přenosu elektronů mezi elektrodou a iontovým druhem, což zvyšuje jejich elektrochemické okno.
Tepelná stabilita a cesty rozkladu: Vnitřní tepelná stabilita disubstituované struktury imidazolu minimalizuje riziko tepelného rozkladu při elektrochemickém napětí, které je často doprovázeno degradací indukovanou napětím. . .



 中文简体
中文简体